El endocardio realiza una función imprescindible, no solo aislando el interior del músculo cardiaco de la sangre que bombea, sino también en la formación de las válvulas cardiacas. Se conoce que el uno por ciento de la población solo desarrolla dos valvas (válvula aórtica bicúspide) en lugar de tres, lo que la hace más proclive a deteriorarse y da lugar a varias patologías cardiovasculares.
Hasta la fecha se han identificado varios genes endocárdicos cuya inactivación conduce a la formación de la válvula aórtica bicúspide y a la enfermedad de la válvula aórtica calcificada. Sin embargo, el conocimiento es muy limitado sobre el papel que desempeñan en el desarrollo de la válvula y la enfermedad las regiones reguladoras endocárdicas no codificantes y los factores ascendentes. Ahora, investigadores del Centro Nacional de Investigaciones Cardiovasculares Carlos III (CNIC) han identificado los mecanismos moleculares que controlan los genes implicados en la correcta formación de estas válvulas y en la prevención de su posterior calcificación. Los hallazgos se publican en la revista ‘Circulation Research’.
Estos hallazgos son relevantes, ya que además de resaltar las vías por las cuales se forma el corazón humano, también ofrecen pistas para futuros avances médicos. “Al comprender estos procesos fundamentales, los científicos se acercan un paso más para resolver los misterios del corazón humano y de sus patologías”, asegura José Luis de la Pompa, jefe del Laboratorio de Señalización Intercelular en el Desarrollo y la Enfermedad Cardiovascular en el CNIC y coordinador del estudio.
Vía de señalización NOTCH
La vía de señalización NOTCH desempeña un papel relevante en las etapas del desarrollo cardiovascular. Los estudios que se han llevado a cabo hasta la fecha han demostrado que cuando esta vía experimenta algún tipo de perturbación es la responsable de la malformación valvular y de la calcificación. NOTCH actúa en el endocardio desde las etapas tempranas del desarrollo hasta la adultez. Se sabe que la presencia de mutaciones en diferentes elementos de esta vía están implicadas en la formación de la válvula aórtica bicúspide.
La presencia de mutaciones en diferentes elementos de la vía de señalización NOTCH están implicadas en la formación de la válvula aórtica bicúspide.
En el nuevo estudio, los investigadores han manipulado la señalización NOTCH en células endocárdicas embrionarias de ratón mediante cocultivo a corto y largo plazo con células estromales OP9, que expresan ligandos Notch e inhibición de la actividad NOTCH. Tras esto se examinó el perfil transcripcional y se generaron modelos in vitro e in vivo con deleciones editadas por CRISPR-Cas9 de varios elementos reguladores no codificantes, validando su potencial regulador.
Este proceso ha permitido describir por primera vez los programas génicos activados e inhibidos por dicha vía en el endocardio, distinguiendo una respuesta temprana y una tardía.
Análisis de datos
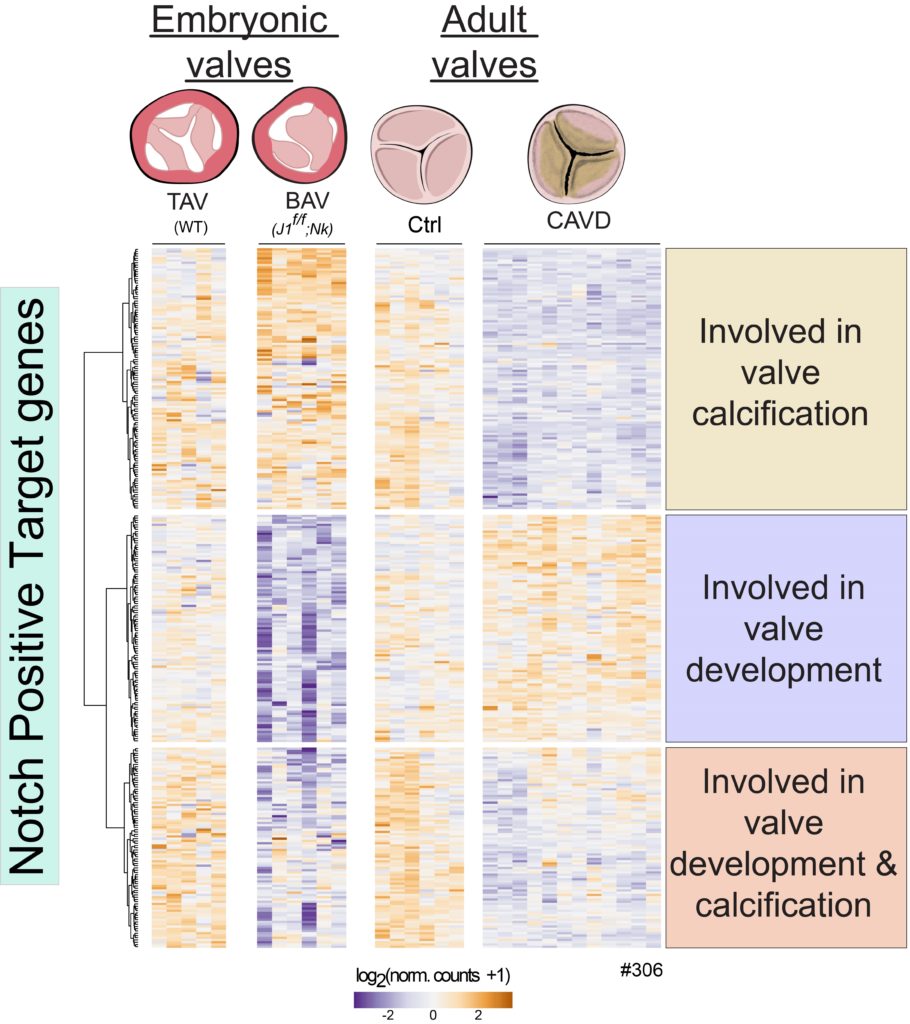
Tras generar los datos de expresión génica, se compararon con programas genéticos previamente descritos por el laboratorio. “Estos datos corresponden al proceso de desarrollo embrionario y calcificación de válvulas adultas, permitiendo la identificación tanto de genes cuyo apagado impide la correcta formación de las válvulas, como aquellos genes cuya inhibición está directamente relacionada con el proceso de calcificación, y genes cuya ausencia afecta negativamente a ambos procesos”, asegura Luis Luna Zurita, autor principal del estudio.
Por otro lado, la investigación ha identificado un conjunto de regiones reguladoras que actúan sobre estos genes. Mientras que los genes suponen el uno por ciento del ADN, es en el 99 por ciento restante donde se encuentran sus regiones reguladoras. Según Luna Zurita, “esto implica que, si la identificación de los genes es muy relevante para entender y tratar la enfermedad, la localización de sus regiones reguladoras lo es igualmente. Analizando los cambios de compactación del ADN, se identificaron aquellas regiones que se abren o cierran tras la actividad de la vía de NOTCH”.
El análisis bioinformático y la integración de diferentes bases de datos de estudios previos ha permitido identificar las regiones del ADN con mayor probabilidad de controlar la expresión de los genes previamente identificados durante la formación y mantenimiento de las válvulas cardiacas, así como las moléculas y vías de señalización encargadas de este control.
“Así hemos descubierto que la cooperación de NOTCH con la vía de señalización HIPPO, una de las vías más estudiadas y crucial para el control de la división celular y el tamaño de los órganos. Este trabajo describe por primera vez la relevancia de la interacción en ambas vías para que el endocardio participe de forma correcta en la formación de las válvulas”, concluye de la Pompa.