La Agencia Española del Medicamento y el Producto Sanitario (Aemps) ha publicado el ‘1º Informe de Farmacovigilancia sobre vacunas COVID-19’. Una de las principales conclusiones es que en la Unión Europea y España no se ha identificado “ninguna posible reacción adversa hasta ahora desconocida que pueda ser motivo de preocupación”.
En el documento se incluyen datos de los acontecimientos adversos sobre vacunas frente a la COVID-19 notificados en España hasta el 12 de enero de 2021. Asimismo, se han incluido respuestas a algunas de las preguntas más frecuentes sobre la seguridad de las vacunas; estas cuestiones se irán actualizando de manera periódica, cuando la Agencia lo estime necesario.
Hasta el 12 de enero de 2021, fecha en que terminó la recogida de datos para el informe estaban autorizadas en la Unión Europea Comirnaty (Pfizer-BioNTech) y COVID-19 Vaccine Moderna. Ambas se están administrando actualmente en España en el marco de la Estrategia de Vacunación; es necesario precisar que desde que comenzara la campaña el 27 de diciembre de 2020 hasta el 12 de enero de 2021, únicamente se estaba administrando la vacuna desarrollada por Pfizer y BioNTech. Por tanto, los datos del informe corresponden a esta vacuna.
Desde España, al igual que en el resto de países de la UE y en coordinación con la Agencia Europea de Medicamentos (EMA) se está realizando una labor de farmacovigilancia exhaustiva. El objetivo es poder detectar nuevas reacciones adversas no identificadas durante los ensayos clínicos de las vacunas frente a la COVID-19.
Acontecimientos registrados
El Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano (SEFV-H) está integrado por los Centros Autonómicos de Farmacovigilancia y coordinado por la Aemps. Este, valora permanentemente los acontecimientos adversos que se notifican en España tras la vacunación, que quedan registrados en la base de datos FEDRA. El objetivo es identificar aquellas nuevas reacciones que puedan surgir, y conocer si realmente están causadas por la vacuna; así, se descarta que se trate de problemas médicos no relacionados que coincidan en el tiempo pero no asociados a la administración de la vacuna.
En total, entre el 27 de diciembre de 2020 y el 12 de enero de 2021 se vacunó a 494.799 personas. El 70 por ciento son mujeres; por edad, el 62 por ciento corresponden a personas de entre 18 y 64 años y el 38 por ciento a mayores de 65. Durante este periodo, se han registrado en FEDRA 374 notificaciones de acontecimientos adversos, lo que se traduce en 79 notificaciones por cada 100.000 personas vacunadas. De estas, el 91 por ciento han sido comunicadas por profesionales sanitarios y el 9 por ciento por el resto de población. En este caso, el 83 por ciento corresponden a mujeres y el 67 por ciento se han registrado entre personas de entre 18 y 64 años.
Desde la Aemps señalan que las 374 notificaciones incluyen 831 términos descriptores de acontecimientos adversos; y es que un mismo caso puede contener varios términos. Por ejemplo, una persona puede haber presentado dolor en el lugar de inyección y fiebre tras la administración de la vacuna.
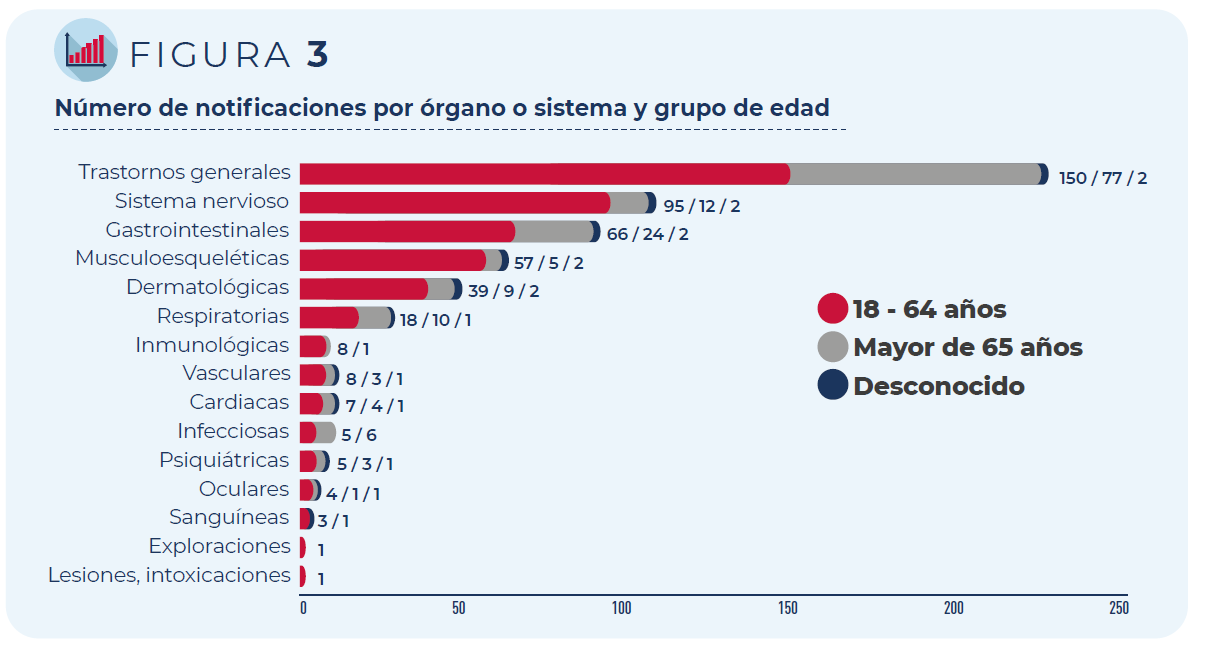
Entre todos los acontecimientos registrados, la fiebre y el malestar general han sido los más frecuentes. Les siguen los trastornos del sistema nervioso (mayoritariamente cefaleas y mareos) y gastrointestinal (principalmente náuseas y diarrea), independientemente del grupo de edad o sexo de las personas vacunadas.
Casos de anafilaxia
Uno de los puntos al que más atención se ha prestado en este informe es a los casos de anafilaxia. Esta reacción adversa es conocida y estaba registrada en la ficha técnica y prospecto de Comirnaty. Sobre este aspecto, una revisión reciente del Center for Disease Control and Prevention de Estados Unidos estima una tasa de anafilaxia de 11.1 casos por millón de dosis administradas, según las notificaciones recibidas que cumplen la definición de anafilaxia. En España solo se han registrado cuatro casos de este acontecimiento; todos ellos en mujeres que se recuperaron o estaban en recuperación tras recibir el tratamiento correspondiente. En 3 de los casos constaban antecedentes personales de reacción alérgica.
La anafilaxia tiene varios signos como la urticaria o eritema generalizado, prurito generalizado con erupción, angioedema, hipotensión, taquicardia, disminución o pérdida de conciencia, sibilancias, estridor, inflamación de las vías respiratorias superiores o dificultad respiratoria. Suele aparecer a los 15-30 minutos tras el contacto con el agente desencadenante y tiene una progresión rápida. Los síntomas pueden llegar a ser graves, por lo que es necesario tratarlo inmediatamente con adrenalina. Desde la Aemps destacan que es importante diferenciar una reacción alérgica de un cuadro vasovagal, ya que comparten algunos síntomas, y de otro tipo de reacciones.
Con el fin de identificar estas reacciones y tratarlas precozmente, desde la Aemps emiten tres recomendaciones. La primera, vigilar la posible aparición de síntomas asociados a la anafilaxia durante al menos 15 minutos tras la administración de la vacuna. Es necesario disponer en los puntos de vacunación de la medicación necesaria para su tratamiento, incluyendo siempre adrenalina, y acceso médico inmediato en caso de que se produzca una reacción alérgica tras la administración de la vacuna. También hay que comprobar que las personas no tengan hipersensibilidad al principio activo o alguno de sus excipientes antes de la vacunación.





































